Fast alle Bodenpartikel der mineralischen und organischen Bodensubstanz sind an ihren Ober- bzw. Grenzflächen elektrisch geladen. Besonders aktiv sind feine Bodenpartikel (Ø < 2 µm), die eine hohe spezifische Oberfläche besitzen und auch als Bodenkolloide bezeichnet werden. Dazu zählen insbesondere Tonminerale und Huminstoffe, aber auch Oxide und Hydroxide im Boden. Bei Tonmineralen und Huminstoffen, die als wesentliche Ladungsträger und Ionenaustauscher gelten, überwiegen die negativen Ladungen.
Aufgrund der elektrischen Ladungsverhältnisse können die Bodenpartikel an ihren Ober- und Grenzflächen Ionen (= elektrisch geladene Teilchen), z.T. auch Atome und Moleküle, aus der Bodenlösung anlagern (= Adsorption ) oder an die Bodenlösung abgeben (= Desorption). Die an den Bodenpartikeln sorbierten Ionen können durch Ionen aus der Bodenlösung verdrängt und ausgetauscht werden. Entsprechend werden Bodenpartikel, die Ionen adsorbieren und austauschen können, als Austauscher bezeichnet.
Der Ionenaustausch vollzieht sich nur zwischen fester und flüssiger Phase, d.h. als Interaktionsprozess zwischen Bodenmatrix (=Festsubstanz) und Bodenlösung. Austauschbar sind alle Ionen, die an den Austauschern sorbiert oder in der Bodenlösung vorhanden sind. Ionen, die im Kristallgitter von Mineralen oder in organischen Substanzen fest gebunden sind, sind nicht austauschbar. Sie können aber z.B. durch Verwitterungs- oder Zersetzungsprozesse mobilisiert werden, ebenso wie die austauschbaren Ionen u.a. durch Mineralneubildungen oder Humifizierungsprozesse immobilisiert werden können. Entsprechend sind die Fraktionen austauschbarer und nicht austauschbarer Ionen permanenten Veränderungen unterworfen (s. Abb. Nährstoffhaushalt des Bodens).
Je nach Ladungsverhältnissen werden die Bodenpartikel bei negativer Ladung als Kationen-Austauscher bzw. bei positiver Ladung als Anionen-Austauscher bezeichnet. In der Regel dominieren im Boden die Kationen-Austauscher, weil die meisten Bodenpartikel vorwiegend negativ geladen sind und dementsprechend überwiegend positiv geladene Ionen (= Kationen ) adsorbieren können.
Die Ionenaustausch-Reaktionen sind reversibel und erfolgen in äquivalenten Mengen, d.h. die an den Austauschern sorbierten Ionen können nur durch ladungsgleiche Ionen äquivalenter Wertigkeit aus der Bodenlösung freigesetzt und ausgetauscht werden (s. Abb.).
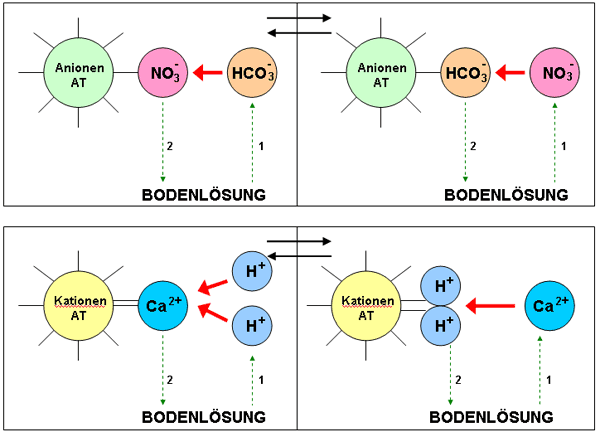 |
Ionenaustauschreaktionen
Diese Ionenaustausch-Fähigkeit des Bodens wirkt sich nachhaltig auf andere Bodeneigenschaften wie z.B. auf den Nährstoffhaushalt des Bodens, die Bodenreaktion, das Bodengefüge und verschiedene Prozesse der Bodenentwicklung. Wie stark dieser Einfluss ist, hängt u.a. von der Austauschkapazität des Bodens ab (s. Kasten 1).
Die Funktion des Bodens als Ionenaustauscher ist
eine wesentliche Voraussetzung für die Versorgung der
Pflanzen mit Nährstoffen.
Diese erfolgt auf der Grundlage von Ionenaustausch-Prozessen
zwischen Bodenpartikeln, Bodenlösung und Pflanzenwurzeln.
Letztere scheiden im Wesentlichen H+- und HCO3--Ionen
aus, die bei der Zellatmung (CO2 + H2O ![]() H2CO3
H2CO3 ![]() H+
+ HCO3-) entstehen, geben sie an die
Bodenlösung
ab und nehmen im Austausch dafür äquivalente Mengen
von Anionen (z.B. NO3-) oder Kationen
(z.B. Ca2+, Mg2+,
K+ oder Na+) aus der Bodenlösung
auf. Diese wiederum interagiert mit den Austauschern (s.
Abb.).
H+
+ HCO3-) entstehen, geben sie an die
Bodenlösung
ab und nehmen im Austausch dafür äquivalente Mengen
von Anionen (z.B. NO3-) oder Kationen
(z.B. Ca2+, Mg2+,
K+ oder Na+) aus der Bodenlösung
auf. Diese wiederum interagiert mit den Austauschern (s.
Abb.).
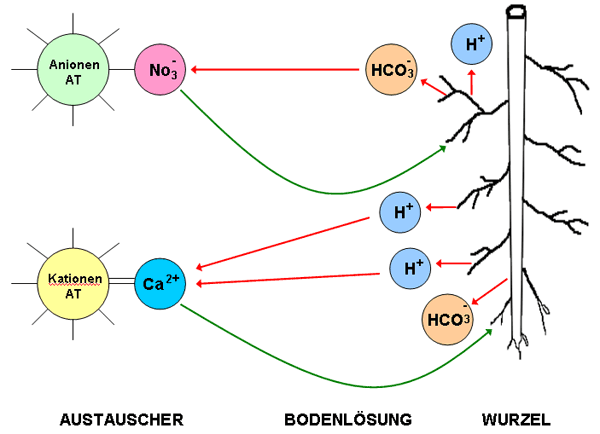 |
Ionenaustausch zwischen Pflanze und Boden
Durch Adsorption der als Nährstoffe fungierenden Ionen an den Austauscher bleiben diese für die Pflanzen leicht verfügbar, wobei gleichzeitig die Auswaschung dieser Ionen mit dem Sickerwasser aus dem Wurzelraum verhindert wird. Von der insgesamt durch Ionenaustausch für die Pflanzen verfügbaren Menge an (Nähr-) Ionen ist in der Regel immer nur ein geringer Anteil in der Bodenlösung vorhanden. Der Hauptanteil ist an den Austauschern sorbiert und kann durch Ionenabgabe der Pflanzenwurzeln über die Bodenlösung eingetauscht werden.
Da viele Ionen, die als Pflanzennährstoffe fungieren, kationisch und die Bodenkolloide überwiegend negativ geladen sind, spielt der Kationen-Austausch im Boden eine herausragende Rolle (s. Kasten 2), während der Anionen-Austausch (s. Kasten 3) eher von untergeordneter Bedeutung ist.
Zu den wichtigsten austauschbaren Kationen im Boden zählen: Ca2+ , Mg2+ , K+ , Na+ sowie Al3+ und H+. Während Al- und H-Ionen die Bodenversauerung (= Bodenacidität ; s. Bodenreaktion) fördern, wirken die Ca-, Mg-, K- und Na-Ionen als basische Gegenspieler. Je stärker sie im Ionenbelag der Austauscher vertreten sind, umso höher ist die Basensättigung der Austauscher und desto besser ist die Pufferung, d.h. die Fähigkeit des Bodens, H+-Ionen zu binden und damit der Bodenversauerung entgegenzuwirken. Die Summe aller austauschbaren Kationen im Boden wird als Kationen-Austauschkapazität (KAK) bezeichnet. Analog zur allgemeinen Austauschkapazität (s. Kasten 1) wird auch hier zwischen maximaler (potentieller) und effektiver (aktueller) KAK differenziert. Höhe der KAK, Zusammensetzung der Ionenbelages an den Austauschern und Basensättigung hängen vom Gehalt der Böden an mineralischen und organischen Austauschern, vom pH-Wert und von der Bodenentwicklung ab. Je höher der Anteil organischer Austauscher im Boden, desto höher ist in der Regel die KAK. Allgemein sind die Kationen
an den Austauschern im Boden unterschiedlich verteilt.
So werden Ca- und Mg-Ionen z.B. stärker von
organischen Austauschern adsorbiert. Darüber
hinaus werden höherwertige Kationen
stärker adsorbiert als geringwertige. Entsprechend
nehmen Eintauschstärke und Haftfestigkeit der
wichtigsten austauschbaren Kationen in folgender Reigenfolge
ab: Analog zu dieser unterschiedlich starken Haftfestigkeit sind in humiden Klimagebieten (Niederschlagsrate > Verdunstungsrate) mit abwärts gerichteter Wasserbewegung Ca- und Mg-Ionen aufgrund ihrer höheren Haftfestigkeit zahlreicher an den Austauschern vertreten als K- und Na-Ionen, die mit dem Sickerwasser leichter ausgewaschen werden können. Grundsätzlich dominieren in schwach sauren bis alkalischen Böden Ca-, Mg-, K- und Na-Ionen im Kationenbelag der Austauscher, während in sauren Mineralböden Al- und H-Ionen überwiegen. |
In Böden mit einem hohen Anteil an Tonmineralen und Huminstoffen spielt der Anionen-Austausch aufgrund der überwiegend negativen Ladungen der Austauscher keine wesentliche Rolle. Hier dominiert der Kationen-Austausch . Im Gegensatz dazu können in oxidreichen Böden mit variablen Ladungen bei steigender Bodenacidität (pH-Wert < 7; s. Bodenreaktion (?)) zunehmend Anionen an den Austauschern gebunden werden. Die Bindung dieser Anionen (z.B. Cl - , NO 3 - , SO 4 2- und PO 4 3- ) ist überwiegend elektrostatischer Natur und die Ionen sind leicht austauschbar. Sobald der pH-Wert der Bodenlösung steigt, geht die positive Ladung der Austauscher verloren und die Anionen werden desorbiert. Insbesondere einwertige Anionen wie Nitrat (NO 3 - )-Ionen, die für die Stickstoffversorgung der Pflanzen wichtig sind, werden dann leicht aus dem Oberboden verlagert und aus dem Boden ausgewaschen. |
Weitere Informationen:
- Nährstoffhaushalt des Bodens
- Bodenreaktion
- Redox-System und Redox-Potential
Literatur:
GISI, U./
SCHENKER, R./ SCHULIN, R./ STADELMANN, F.X./ STICHER, H.
(1997): Bodenökologie
- 2. Auflage - Stuttgart; New York: Thieme.
Scheffer, F./
Schachtschabel, P. (2002): Lehrbuch der Bodenkunde - 15.
Auflage -. Heidelberg; Berlin: Spektrum Akademischer Verlag.
Schroeder, D. (1992):
Bodenkunde in Stichworten - 5. Auflage - Berlin; Stuttgart:
Borntraeger.