Böden enthalten zahlreiche Reduktions- und Oxidations-Systeme, in denen gekoppelte Reduktions- und Oxidationsprozesse ablaufen wie z.B. Ammonifikation (= Reduktion von Nitrat zu Ammonium) und Nitrifikation (= Oxidation von Ammonium zu Nitrit und Nitrat).
Insbesondere in der Bodenlösung finden ständig solche Oxidations- und Reduktionsprozesse (= Redox-Reaktionen) statt. Bei der Oxidation werden Elektronen abgegeben, z.B. durch die Bindung von Sauerstoff-Ionen und/oder Abgabe von Wasserstoff-Ionen, bei der Reduktion Elektronen aufgenommen. Ein Beispiel:
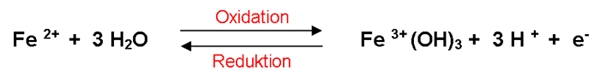 |
Da bei Oxidationsprozessen Wasserstoff(H+)-Ionen produziert und bei Reduktionsprozessen wieder gebunden werden, wirken sich Redox-Reaktionen grundsätzlich auf die Bodenreaktion aus.
Als Maß für die oxidierende bzw. reduzierende Kraft eines Redox-Systems gilt das Redox-Potential (E). Es bezeichnet das elektrische Potential (in Millivolt (mV)), das durch den Elektronentransport vom Elektronen-Donator zum Elektronen-Akzeptor entsteht. Ein hohes Redox-Potential korreliert mit einer starken Oxidationskraft im Redox-System. Im Boden variieren die Redox-Potentiale zwischen -300 mV (= stark reduzierende Verhältnisse) und +800 mV (= stark oxidierende Verhältnisse).
Hohe Redox-Potentiale, die mit einem Überwiegen von Oxidationsprozessen einhergehen, sind kennzeichnend für gut belüftete und sauerstoffreiche Böden mit großen Anteilen von oxidierten Verbindungen (z.B. Fe- und Mn-Oxide/-Hydroxide, Nitrate, Sulfate) und weitgehendem Abbau der leicht umsetzbaren organischen Substanz. Böden mit Sauerstoffmangel und einer Anreicherung leicht abbaubarer organischer Substanz dagegen zeichnen sich durch ein niedriges Redox-Potential aus. Das gilt insbesondere für Grund- und Stauwasser- sowie Überflutungsböden.
Atmungsprozesse aerober Bodenorganismen, die Sauerstoff verbrauchen, und Reduktionsprozesse anaerober Mikroorganismen verursachen eine Erniedrigung des Redox-Potentials. Parallel dazu steigen die pH-Werte (s. Bodenreaktion), da bei Reduktionsprozessen Wasserstoff-Ionen gebunden werden (s.o.). Umgekehrt sinkt mit steigendem Redox-Potential der pH-Wert, weil durch Oxidationsprozesse Wasserstoff-Ionen produziert werden.
Insgesamt gesehen beeinflusst das Redox-Potential verschiedene pedogenetische Prozesse wie z.B. die Oxidationsverwitterung, Verwesung, Bodenfärbung und Bodenbildungsprozesse. Darüber hinaus ist es von ökologischer Bedeutung, insbesondere im Hinblick auf die Verfügbarkeit oxidier- und reduzierbarer Nährelemente wie N, S, Fe, Mn und Mo (s. Nährstoffhaushalt) oder die Freisetzung löslicher Phosphate (durch Reduktion von FeIII-Hydroxid-Phosphat-Komplexen; s. SCHROEDER 1992, S. 82).
Bei niedrigen Redox-Potentialen
liegen die meisten Elemente und Verbindungen in niedrigeren
Oxidationsstufen vor und weisen in der Regel eine höhere Löslichkeit auf.
Damit sind sie leichter verfügbar für die Pflanzen,
können aber auch schneller aus dem Boden ausgewaschen
werden oder mit anderen Verbindungen reagieren.
Weitere Informationen:
- Nährstoffhaushalt
- Ionenaustausch und Austauschkapazität
- Bodenreaktion
Literatur:
Gisi, U./
Schenker, R./ Schulin, R./ Stadelmann, F.X./ Sticher, H.
(1997): Bodenökologie
- 2. Auflage - Stuttgart; New York: Thieme.
Hintermaier-Erhard,
G./ Zech, W. (1997): Wörterbuch
der Bodenkunde. Stuttgart: Enke.
Scheffer, F./ Schachtschabel,
P. (2002): Lehrbuch der Bodenkunde - 15. Auflage -. Heidelberg;
Berlin: Spektrum Akademischer Verlag.
Schroeder, D. (1992):
Bodenkunde in Stichworten - 5. Auflage - Berlin; Stuttgart:
Borntraeger.